Butantan entrega à Anvisa dados sobre a Coronavac para iniciar registro da vacina
De acordo com o Butantan, a expectativa é que os 9.000 voluntários que participam dos testes da Coronavac no Brasil sejam vacinados ainda em outubroO governador de São Paulo, João Doria (PSDB), disse nessa sexta-feira (2) que o Instituto Butantan entregou à Anvisa (Agência Nacional de Vigilância Sanitária) a documentação existente sobre a Coronavac. A vacina, da fabricante chinesa Sinovac, está na fase 3 de testes.
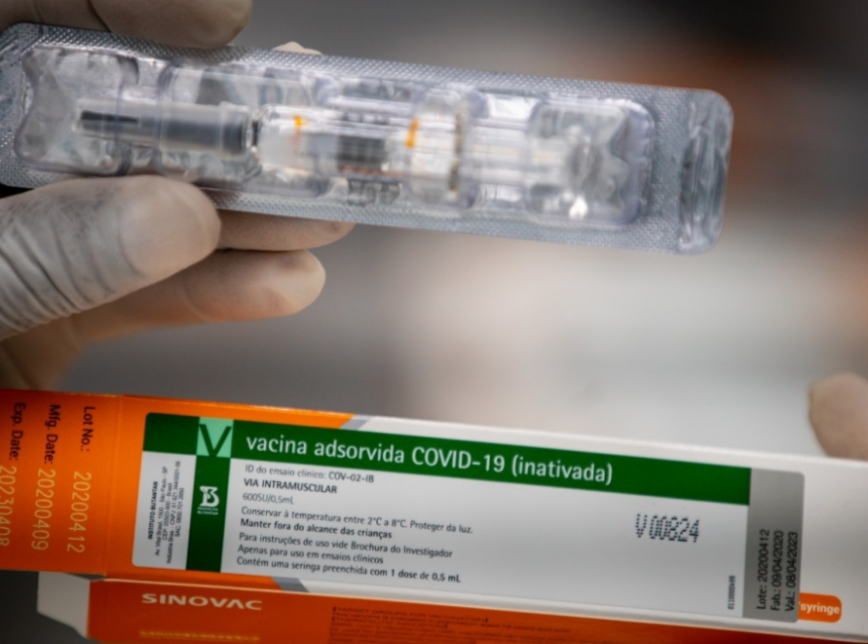
A entrega da documentação é um dos passos para o registro do imunizante junto à Anvisa (Agência Nacional de Vigilância Sanitária), necessário para a vacinação em massa da população.
“O governo de São Paulo registrou na Anvisa a documentação da Coronavac para análise e obtenção do registro”, afirmou Doria. “Nosso objetivo é tornar esse processo mais rápido, mas sempre dentro das normas científicas, seguindo todos os protocolos.”
O Butantan entregou uma avaliação de dados preliminares e os relatórios de eficácia e segurança obtidos até o momento com a Coronavac em testes não-clínicos (feitos em laboratório ou em animais antes da testagem em humanos).
A Anvisa criou um novo procedimento regulatório para as vacinas contra a COVID-19, chamado de submissão contínua. A agência analisa os dados à medida em que eles chegam, “até que evidências suficientes estejam disponíveis para suportar UM pedido formal de registro”. A área técnica do órgão já está avaliando o primeiro conjunto de informações sobre a vacina desenvolvida pela AstraZeneca em parceria com a Universidade de Oxford.
De acordo com o Butantan, a expectativa é que os 9.000 voluntários que participam dos testes da Coronavac no Brasil sejam vacinados ainda em outubro. Se a vacina for bem-sucedida, o instituto vai pedir aprovação emergencial do imunizante.
Na quarta-feira (30), o gerente-geral de medicamentos e produtos biológicos da Anvisa, Gustavo Mendes Lima Santos, falou que a agência pode flexibilizar os critérios de eficácia para aprovação de uma vacina contra a COVID-19.
Em reunião da Comissão Externa de Enfrentamento à COVID-19 na Câmara dos Deputados, ele disse que o órgão pode liberar um imunizante com 50% de eficácia mínima. O padrão é que o número seja acima de 70%.
Segundo ele, a exceção é possível uma vez que não existe um dispositivo normativo que estabeleça o critério. “Nós usamos tradicionalmente 70%, mas estamos dispostos, em um compartilhamento com outras agências reguladoras, numa decisão técnica com outras agências, a flexibilizar esses critérios tendo em vista esse cenário [de pandemia]”, disse Santos.
Fonte: Poder360
Comentários
Últimas Notícias
-
 Cultura
Centro Cultural do Tribunal Regional Eleitoral do Piauí é inaugurado em Teresina
Cultura
Centro Cultural do Tribunal Regional Eleitoral do Piauí é inaugurado em Teresina
- Eventos Convocada assembleia de fundação da Associação dos Policiais Penais e Agentes de Segurança Pública do Estado do Pará
-
 Geral
Povoado Peixe em Massapê do Piauí comemora início da obra de calçamento autorizada pela Secretaria do Agronegócio
Geral
Povoado Peixe em Massapê do Piauí comemora início da obra de calçamento autorizada pela Secretaria do Agronegócio
-
 Justiça
Sociedade Contemporânea: Congresso Internacional de Relações de Trabalho alerta sobre precarização do trabalho
Justiça
Sociedade Contemporânea: Congresso Internacional de Relações de Trabalho alerta sobre precarização do trabalho
-
 Justiça
Valor de seguro de vida resgatável pode ser penhorado quando sacado pelo próprio segurado, decide STJ
Justiça
Valor de seguro de vida resgatável pode ser penhorado quando sacado pelo próprio segurado, decide STJ


